Introducción
El dengue es una infección arboviral transmitida comúnmente por la picadura de un mosquito infectado. El vector principal es Aedes aegypti, un mosquito doméstico que pica durante el día y se reproduce en recipientes de agua en zonas peridomésticas; sus huevos pueden sobrevivir sin desecación en estado seco durante meses, y con el primer contacto con el agua comienza su ciclo biológico. Cuenta con una incidencia creciente en los últimos años que pone en riesgo a casi la mitad de la población mundial1. En México, el dengue es una de las principales enfermedades transmitidas por vectores, y en los últimos 10 años ha incrementado el número de casos a pesar de los esfuerzos de prevención y control del vector2. La caracterización clínica del dengue es muy variable debido a las múltiples alteraciones inducidas por el virus en el organismo. Se ha reportado un incremento en los niveles de transaminasas similar al producido por el virus de la hepatitis. La clasificación realizada por la Organización Mundial de la Salud (OMS) en 1997 fue revisada a partir de 2004, y la que se encuentra en uso desde 2009 lo clasifica en: 1) dengue no grave, que a la vez se subdivide en pacientes con o sin signos de alarma, y 2) dengue grave. Después del periodo de incubación, el dengue inicia de manera súbita cursando en tres fases: febril (2.o a 7.o días), crítica (24 a 48 horas) y de recuperación3.
En los donantes vivos provenientes de áreas no endémicas puede evaluarse el riesgo de exposición mediante la detección de viajes recientes, así como educarles para evitar infecciones previas a la donación. En contraste, los donantes de regiones endémicas deben diferirse si tienen antecedentes recientes de una enfermedad febril sugestiva de infección activa por arbovirus, particularmente dentro de los 30 días previos. En donantes vivos que se hayan aplicado recientemente la vacuna contra el dengue de virus atenuado, se deberá esperar al menos 30 días desde el momento de la aplicación para proceder con el trasplante. Se recomienda obtener y guardar suero de donantes provenientes de zonas de alto riesgo para el dengue con el fin de realizar serología ante la aparición de signos o síntomas sugestivos de esta enfermedad en el receptor4.
Caso clínico
Mujer de 43 años con los siguientes antecedentes personales patológicos de importancia: enfermedades crónicas degenerativos negadas, alergia a la penicilina, una cesárea hace 9 años (sin complicaciones), nefrectomía laparoscópica asistida manualmente de donante 2 semanas antes, hemotipo O+, gesta 4, partos 1, aborto 1. Inició protocolo hace 6 meses para potencial donante vivo relacionado (madre) de injerto renal, efectuándose en el mes de agosto, sin complicaciones. Se registraron exámenes de laboratorio previo y posterior al trasplante renal, con determinación de hemoglobina, hematocrito, creatinina, plaquetas, pruebas de función hepática con bilirrubina total, bilirrubina directa, bilirrubina indirecta, fosfatasa alcalina, deshidrogenasa láctica, gamma glutamil transpeptidasa, aspartato aminotransferasa y alanino aminotransferasa, tiempo de protrombina, INR (International Normalized Ratio) y tiempo parcial de tromboplastina (Tabla 1). A la semana, acudió a consulta de revisión posoperatoria presentando cefalea, hipoacusia izquierda y eritema faríngeo. Nuevamente, a los 4 días, refirió persistencia de náusea, emesis de contenido gástrico, uresis conservada, ausencia de dolor abdominal o dolor subcostal, y un pico febril no cuantificado. Se tomaron laboratorios de control que evidenciaron elevación de las enzimas hepáticas, plaquetopenia y neutropenia, lo que motivó su atención hospitalaria. A los 3 días de hospitalización presentó exantema cutáneo generalizado acompañado de prurito (Fig. 1). El perfil TORCH reportó anticuerpos anti-Ag de cápside Epstein-Barr VCA (IgG) 30.6 AU/ml, anti-Epstein Barr VCA (cápside) (IgM) < 0.01 AU/ml, anti-herpes virus 1 y 2 (IgM) 0.0 AU/ml, HIV Ag/Ab 0.16 UI/ml, HBsAg 0.33 UI/l, anti-HCV 0.04 COI, anti-rubeola (IgM) 0.298 COI, anti-rubeola (IgG) 45.70 UI/ml, anti-CMV (IgM) 0.297 COI, anti-CMV (IgG) 411.9 U/ml, y VDRL negativo. Fracción C3 del complemento 81.0 mg/dl, fracción C4 del complemento 7.17 mg/dl, IgM 271 mg/dl, IgA 221 mg/dl, IgG 1036 mg/dl, anti-Ro IgG SS-A Ac < 4.9 CU (negativo), antinucleares negativo, ANCA-C antiproteinasa 3 IgG < 2.3 CU, ANCA-P antimieloperoxidasa < 3.2 CU, IgG contra cardiolipina < 2.6 CU, IgM contra cardiolipina 54.20 CU, anti-Smith IgG < 3.3 CU, anti-La IgG SS-B < 3.3 CU y antimúsculo liso negativos.
Tabla 1. Seguimiento de los estudios de laboratorio
| Parámetro | Día 0 | Día 2 | Día 7 | Día 9 | Día 11 | Día 12 | Día 13 | Día 14 | Día 15 | Día 16 | Día 18 |
|---|---|---|---|---|---|---|---|---|---|---|---|
| Hemoglobina (mg/dl) | 12.9 | 9.9 | 11.6 | 13.0 | 14.8 | 11.3 | 11.0 | 10.5 | 10.5 | 11.9 | 11.4 |
| Hematocrito (%) | 37.4 | 28.6 | 34.3 | 39.0 | 43.5 | 32.9 | 32.0 | 30.4 | 30.5 | 34.9 | 34.9 |
| Plaquetas (× 103/µl) | 226 | 167 | 206 | 157 | 76 | 45 | 70 | 104 | 175 | 307 | 457 |
| Creatinina (mg/dl) | 1.0 | 1.0 | 1.0 | 1.1 | 1.1 | 1.1 | 1.0 | – | 0.9 | 1.1 | 1.0 |
| BD (mg/dl) | 0.25 | 0.2 | 0.23 | 0.18 | 0.29 | 0.19 | 0.24 | 0.18 | 0.15 | 0.16 | 0.14 |
| BI (mg/dl) | 0.3 | 0.2 | 0.2 | 0.17 | 0.19 | 0.14 | 0.16 | 0.16 | 0.09 | 0.17 | 0.11 |
| BT (mg/dl) | 0.55 | 0.4 | 0.43 | 0.35 | 0.48 | 0.33 | 0.40 | 0.34 | 0.24 | 0.33 | 0.25 |
| FA (U/l) | 46.6 | 55.8 | 161 | 170 | 261 | 197 | 184 | – | 156 | 167 | 162 |
| DHL (U/l) | – | 191 | – | 482 | 898 | 456 | – | – | 314 | 329 | 317 |
| AST (U/l) | 128 | 103 | 293 | 435 | 1280 | 699 | 545 | 372 | 282 | 255 | 149 |
| ALT (U/l) | 103 | 161 | 487 | 516 | 935 | 575 | 482 | 374 | 339 | 321 | 237 |
| GGT (U/l) | 47.1 | 60.7 | 207 | 202 | 484 | 435 | 397 | – | 343 | 352 | 307 |
| TP (s) | 12.0 | – | 11.5 | – | 10.1 | 9.4 | – | 9.9 | – | – | – |
| INR | 1.0 | – | 1.0 | – | 0.8 | 0.8 | – | 0.8 | – | – | – |
| TPTa (s) | 30.8 | – | 36.4 | – | 44.0 | 37.2 | – | 31.6 | – | – | – |
|
ALT: alanino aminotransferasa; AST: aspartato aminotransferasa; BD: bilirrubina directa; BI: bilirrubina indirecta; BT: bilirrubina total; DHL: deshidrogenasa láctica; FA: fosfatasa alcalina; GGT: gamma glutamil transpeptidasa; INR: International Normalized Ratio; TP: tiempo de protrombina; TPTa: tiempo parcial de tromboplastina. |
|||||||||||
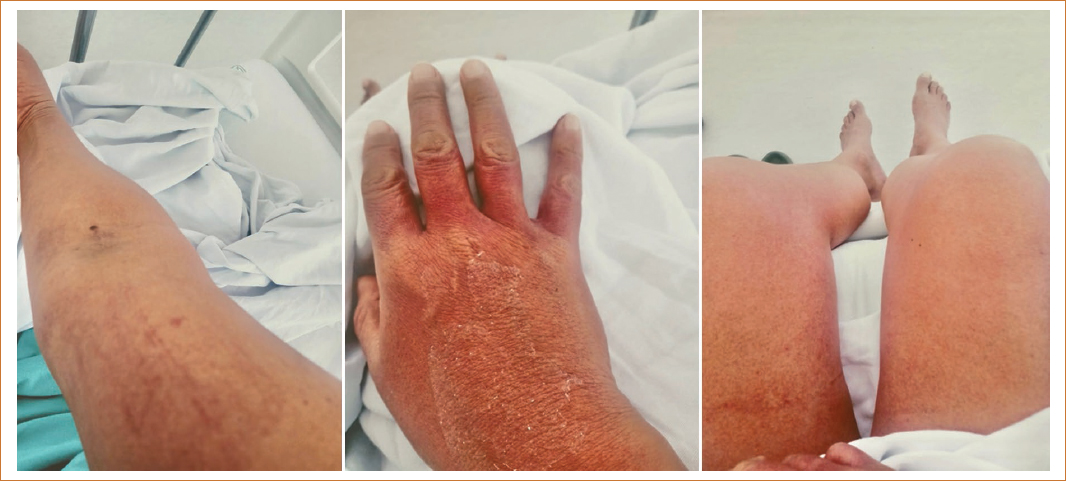
Figura 1. Manifestaciones dermatológicas: exantema rojizo intenso de predominio en las extremidades superiores e inferiores acompañado de prurito.
Se transfundió una aféresis plaquetaria el 17/08 al presentar sangrado transvaginal y plaquetopenia de 45.0 × 103/μl. Se solicitó ensayo de Zika/Dengue/Chikungunya, con prueba positiva reportada el 19/08 (Tabla 2). Fue dada de alta a los 5 días por mejoría de las enzimas hepáticas, la plaquetopenia y la leucocitopenia. Actualmente con resolución de la plaquetopenia y de la leucocitopenia, y disminución de las enzimas hepáticas, por lo cual se continuará manejo ambulatorio con hidratación por vía oral.
Tabla 2. Resultados del ensayo de Zika/Dengue/Chikungunya
| Ensayo | Kit/equipo | Fecha de resultado | Resultado |
|---|---|---|---|
| Detección simultanea de RNA del virus Zika por PCR múltiple en tiempo real | TAQMANTM MULTIPLEX KIT (ZIKV/DENV/CHIKV) | 19/08 | Negativo |
| Detección simultánea de RNA del virus Chikungunya por PCR múltiple en tiempo real | TAQMANTM MULTIPLEX KIT (ZIKV/DENV/CHIKV) | 19/08 | Negativo |
| Detección simultánea de RNA del virus de dengue por PCR múltiple en tiempo real | TAQMANTM MULTIPLEX KIT (ZIKV/DENV/CHIKV) | 19/08 | Positivo |
| Tipificación de los serotipos de dengue por PCR en tiempo real | VIASURE Dengue Serotyping Real Time PCR Detection Kit | 19/08 | DENV 3 |
|
PCR: reacción en cadena de la polimerasa. |
|||
Discusión
El dengue constituye un problema de salud pública, principalmente en zonas endémicas, caracterizado por manifestaciones clínicas que varían desde cuadros febriles autolimitados hasta formas graves con compromiso multiorgánico. La mayor parte de la literatura se enfoca en pacientes receptores de injerto renal, en quienes la inmunosupresión desempeña un papel muy importante ya que incrementa el riesgo de complicaciones y de mortalidad. Sin embargo, la presentación del dengue en donadores de injerto renal es un escenario poco investigado, lo que hace relevante el análisis del presente caso. Los donantes renales suelen ser individuos sanos y con la nefrectomía pierden la mitad de su masa renal; se estima que el riñón remanente compensa idóneamente un 70% de la función renal previa a la donación5, aunque existe la posibilidad de aumentar la vulnerabilidad frente a la deshidratación, fuga capilar y trombocitopenia tras presentarse la infección. Por lo tanto, se resaltan la importancia y la necesidad de vigilancia estrecha ante datos de alarma, reposición hídrica adecuada y monitoreo estricto de la función renal y hemostasia en quienes han sido sometidos a cirugía recientemente. Se ha descrito que el virus del dengue puede producir disfunción hepática moderada, e incluso casos graves con elevación importante de las transaminasas, la bilirrubina y la fosfatasa alcalina, llegando incluso a valores similares a los de una hepatitis viral. El estudio de las alteraciones hepáticas en pacientes infectados con el virus del dengue tiene especial relevancia en la caracterización clínica de esta enfermedad, ya que con frecuencia se presentan signos y síntomas de disfunción hepática y se plantean otros diagnósticos clínicos, no como parte de un mismo proceso patogénico6. Aunque este escenario es infrecuente, indica la necesidad de realizar un tamizaje clínico y epidemiológico de los donadores en áreas endémicas, principalmente en periodos de brote. La Sociedad Argentina de Infectología recomienda que los potenciales donantes que provengan de zonas epidémicas o endémicas de dengue deberían ser testeados con prueba de antígeno dengue NS1 o con pruebas de detección genómica (reacción en cadena de la polimerasa [PCR]) para detectar viremia, y con IgM si pasaron más de 5 días desde el comienzo de un cuadro compatible. Si el donante tiene positivo el NS1 o la detección genómica por PCR es positiva, debe descartarse como donante. En caso de IgM positiva, si se desconoce el tiempo de inicio de los síntomas o este es < 30 días, también se deberá descartar. Asimismo, se recomienda obtener y guardar suero de donantes provenientes de zonas de alto riesgo para dengue con el fin de realizar serología ante la aparición de signos o síntomas sugestivos de esta enfermedad en el receptor o en el mismo donante7.
Conclusión
La infección por dengue en donadores de injerto renal constituye una condición poco frecuente y estudiada, pero con importantes implicaciones clínicas y éticas. El caso presentado destaca la necesidad y la importancia de realizar pruebas diagnósticas de tamizaje en regiones endémicas, así como una vigilancia estrecha del donador, medidas profilácticas y manejo de soporte individualizado, para garantizar la seguridad tanto del donador como del receptor.
Financiamiento
Los autores declaran que este trabajo se realizó con recursos propios.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. Los autores han obtenido la aprobación del Comité de Ética para el análisis de datos clínicos obtenidos de forma rutinaria y anonimizados. Debido a la naturaleza del estudio, no fue necesario el consentimiento informado individual. Se han seguido las recomendaciones éticas pertinentes.
Declaración sobre el uso de inteligencia artificial (IA). Los autores declaran que no se utilizó ningún tipo de inteligencia artificial generativa para la redacción ni la creación de contenido de este manuscrito.
