Introducción
En México, la enfermedad cardiovascular (ECV) es la principal causa de mortalidad (el 20.1% de todas las muertes), siendo la cardiopatía isquémica (76.3%) la afección predominante1,2. Los factores de riesgo (FR) cardiovascular (CV) están presentes en el 70% de la población adulta mexicana3,4. La diabetes tipo 2 (DT2) aumenta de dos a cuatro veces el riesgo de desarrollar ECV4 y es causa de mortalidad en alrededor del 50% de los pacientes con DT25,6.
En México en el periodo de 1998 a 2014 se ha reportado un incremento en la morbimortalidad relacionada con la enfermedad renal crónica (ERC) del 118% y en 2017, una prevalencia de ERC del 12.2%7–9. La DT2 y sus complicaciones cardiorrenales tienen un impacto económico significativo, Figueroa-Lara et al. reportaron que la ERC, hipertensión arterial (HTA), la DT2 y la cardiopatía isquémica crónica representaron del 85 al 88% de la carga económica total de las enfermedades crónicas en el sector salud10. En 2021, la carga económica por la DT2 se estimó en 19.9 billones de dólares (IDF), siendo la mayoría de los costos (87%) atribuibles a complicaciones11. Para disminuir la carga de la enfermedad es importante el manejo integral, la búsqueda activa de riesgo cardiorrenal al momento del diagnóstico y el seguimiento4,5,12,13. Las guías de la Sociedad Europea de Cardiología (ESC) 2019 incluyen la identificación de FR CV y la presencia de daño a órgano blanco por diabetes como elementos centrales para la toma decisiones clínica según el perfil de riesgo individual obtenido en cada paciente. El papel de la albúmina urinaria como indicador de daño renal y marcador de riesgo cardiorrenal es ampliamente reconocido, y las guías de atención sugieren su medición para la identificación oportuna de este riesgo14. El objetivo de este estudio fue determinar el riesgo CV y la prevalencia de los factores de riesgo cardiorrenal en pacientes mexicanos con DT2 sin antecedentes de enfermedad CV o renal establecidas, en el primer nivel de atención.
Método
Tipo de estudio
Análisis de cohorte prospectivo, observacional, dirigido por médicos de atención primaria.
Periodo
Diciembre de 2020 a octubre de 2021.
Variables
Se capturaron las características demográficas, antecedentes, evolución clínica, pruebas diagnósticas y tratamientos de pacientes con DT2, los registros se realizaron en la plataforma electrónica (iCaReMe Registry)15, la cual es una base de datos del programa multinacional Take Care of Me (TCoM). Se realizó historia clínica, examen físico y mediciones de hemoglobina glucosilada (HbA1c), perfil lipídico, relación albúmina: creatinina urinaria (RACU), edad, índice de masa corporal (IMC), duración de la DT2, presión arterial sistólica (PAS), colesterol vinculado a lipoproteínas de alta densidad (c-HDL), colesterol vinculado a lipoproteínas de baja densidad (c-LDL) y triglicéridos. Los valores de los lípidos estuvieron tomados de acuerdo con las guías ATP 4 (colesterol total elevado ≥ 200 mg/dl o más, triglicéridos elevados ≥ 150 mg/dl, c-LDL elevado ≥ 100 mg/dl, c-HDL disminuido < 40 mg/dl). El riesgo CV se evaluó basado en guía clínica 2019 de la ESC y la Sociedad Europea para el Estudio de la Diabetes12, la cual integra además de la edad y el tiempo con el diagnóstico de DT2, la presencia de FR CV (edad, hipertensión, dislipidemia, tabaquismo, obesidad) y de daño a órgano blanco (proteinuria, ERC definida por tasa de filtración glomerular (TFG) estimada ≤ 30 ml/min/1.73m2), estratificando a los pacientes en las categorías de riesgo moderado, alto o muy alto. Al subgrupo de pacientes con alto o muy alto riesgo CV dependiendo de la disponibilidad y evaluación clínica se les realizó un ecocardiograma.
El riesgo de enfermedad renal se determinó por medio de la RACU en una muestra al azar. Los resultados se clasificaron de acuerdo con el grado de albuminuria en A1 (< 30 mg/g), A2 (30 a 300 mg/g) y A3 (> 300 mg/g)13.
Se aplicó un modelo de recursos mínimos para predecir una TFG disminuida, desarrollado por Gendius y descrito en Sammut-Powell et al., que utiliza edad, sexo, IMC, duración de la DT2 y mediciones de la presión arterial. El modelo estratifica el riesgo en siete categorías y niveles en donde 4 a 7 indican riesgo de TFG < 60%16.
Criterios de inclusión y no inclusión
- – Criterios de inclusión: este registro se abrió a médicos en todo el mundo. Esta investigación utilizó la cohorte de pacientes mexicanos de seis clínicas privadas de atención primaria en los estados de Jalisco (Mariano Otero, Circunvalación y Tlaquepaque) y Nuevo León (Clínica de la Fé, Guadalupe y Lincoln).
- – Criterios de no inclusión: se excluyeron pacientes con DT1, pacientes que participaran en cualquier protocolo intervencional o la presencia de comorbilidades graves (cualquier comorbilidad que comprometiese la vida y con una expectativa de vida menor a un año con base en el juicio médico).
Se incluyeron pacientes ≥ 18 años de edad, con DT2, sin antecedentes de ERC o ECV.
Aprobación
En todas las clínicas se obtuvo la aprobación del comité de ética e investigación local.
Todos los pacientes firmaron el consentimiento informado.
Análisis estadístico
Se realizó un análisis descriptivo, las variables continuas se describen con mediana y primer y tercer cuartiles, las categóricas mediante frecuencias y porcentajes. Se aplicó un modelo de regresión logística para evaluar la asociación de factores con el RCV. Se incluyeron los factores con un valor de p < 0.20 para análisis univariantes, aplicando prueba de Wald y presentados como razón de momios (RM) a intervalos de confianza del 95% [IC 95%]. La construcción del modelo estadístico se guio por el criterio de Akaike y la generalidad de los resultados. Se consideró un valor significativo con p < 0.05.
Resultados
Se incluyeron 2,761 sujetos. El 96.4% se categorizó en riesgo CV alto y muy alto (63.4 y 33.0%, respectivamente) y 98 (3.5%) con riesgo moderado. La albuminuria en etapas A2-A3 se encontró en 658 pacientes (24.5%) y 1,865 presentaron HbA1c > 7% (68.8%) (Tabla 1).
Tabla 1. Características de los participantes de acuerdo con el nivel de riesgo cardiovascular
| Riesgo | Moderado n = 98 (3.5%) | Alto n = 1,751 (63.4%) | Muy alto n = 912 (33.0%) | Población total n = 2,761 (100%) |
|---|---|---|---|---|
| Mediana (Q1-Q3) | Mediana (Q1-Q3) | Mediana (Q1-Q3) | Mediana (Q1-Q3) | |
| Edad, años | 40.5 (34.2-44.7) | 54 (47-61) | 55 (47-63) | 54 (46-61) |
| Índice de masa corporal, kg/m2 | 26.8 (24.8-28.5) | 29.1 (26.1-32.8) | 30.6 (26.7-34.6) | 29.3 (26.2-33.3) |
| Duración DT2, años | 1.9 (0.9-4.9) | 5.9 (1.9-11.9) | 7.9 (2.9-15.9) | 5.9 (1.9-11.9) |
| < 5 años | 76 (77.5%) | 830 (47.7%) | 338 (37.2%) | 1244 (45.3%) |
| 5 a 10 años | 22 (22.4%) | 381 (21.9%) | 198 (21.8%) | 601 (21.9%) |
| > 10 años | 526 (30.2%) | 372 (40.9%) | 898 (32.7%) | |
| Presión arterial sistólica, mmHg | 110 (100-120) | 120 (110-120) | 120 (110-130) | 120 (110-120) |
| Relación albúmina: creatinina en orina, mg/g | 8.6 (5.8-14.1) | 8.9 (6-14.0) | 53.3 (24.3-141.5) | 12.2 (6.8-29.4) |
| Estadio albuminuria A1 | 92 (100%) | 1679 (100%) | 242 (26.8%) | 2013 (75.3%) |
| Estadio albuminuria A2 | 565 (62.7%) | 565 (21.1%) | ||
| Estadio albuminuria A3 | 93 (10.3%) | 93 (3.4%) | ||
| HbA1c, % | 7.8 (6.5-10.3) | 7.7 (6.7-9.8) | 8.6 (7.1-11.1) | 8 (6.8-10.4) |
| < 7 | 35 (36.8%) | 597 (34.8%) | 210 (23.3%) | 842 (31.1%) |
| 7.1-10 | 34 (35.7%) | 710 (41.4%) | 366 (40.7%) | 1110 (41.0%) |
| > 10 | 26 (27.3%) | 407 (23.7%) | 322 (35.8%) | 755 (27.8%) |
| c-HDL, mg/dl | 42 (35-49) | 41 (33-48) | 41 (33-50) | 41 (33-49) |
| c-LDL, mg/dl | 75.5 (55.7-103.4) | 76 (50.7-105) | 80 (53-108) | 78 (51.6-105.2) |
| Colesterol total, mg/dl | 150 (120.4-168) | 153 (118-186) | 162 (123-198.5) | 156 (120-189) |
| Triglicéridos, mg/dl | 125 (99-148) | 148 (113-191) | 159.5 (122-220) | 150 (115-199) |
|
*Los datos se presentan como mediana (percentiles 25-75). c-HDL: colesterol vinculado a lipoproteínas de alta densidad; c-LDL: colesterol vinculado a lipoproteínas de baja densidad; DT2: diabetes tipo 2; HbA1c: hemoglobina glucosilada. |
||||
Las cifras de colesterol total elevado se presentaron en 464 (17.5%), 1,410 (56.3%) con c-LDL elevado, 1,330 (49.1%) con c-HDL bajo, y 1,343 con triglicéridos incrementados (49.7%).
La PAS ≥ 130 mmHg se reportó en 569 (20.5%), el IMC de 25 a 30 en 1,040 (38.2%) y > 30 en 1,226 (45%), 2,295 participantes (83.1%) estaban en tratamiento para diabetes, 1,060 (38.3%) en monoterapia. Recibieron biguanidas 2,090 (75.7%) de forma única o en combinación. Los antidiabéticos con beneficio CV estaban prescritos en 426 (15.3%), de los cuales el 98.1% fueron inhibidores del cotransportador sodio-glucosa tipo 2 (iSGLT-2) y el 1.87% agonistas del receptor del péptido similar a glucagón (arGLP-1). El uso de insulina fue del 34.1% (Tabla 2).
Tabla 2. Medicamentos para el tratamiento de la diabetes tipo 2 según el riesgo cardiovascular
| Terapéutica | Riesgo cardiovascular | |||||||
|---|---|---|---|---|---|---|---|---|
| Moderado | Alto | Muy alto | Total | |||||
| n | % | n | % | n | % | n | % | |
| Con antidiabético | 75 | 76.53 | 1,462 | 83.50 | 758 | 83.11 | 2,295 | 83.12 |
| Con antidiabético con beneficio CV | 9 | 9.1 | 271 | 15.5 | 146 | 16.1 | 426 | 15.3 |
| Biguanida | 62 | 63.3 | 1339 | 76.5 | 689 | 75.5 | 2090 | 75.7 |
| Sulfonilurea | 13 | 13.3 | 359 | 20.5 | 185 | 20.4 | 557 | 20 |
| Inhibidores α-glucosidasa | 0 | 0 | 0 | 0 | 3 | 0.3 | 3 | 0.1 |
| Agonista PPAR-y | 0 | 0 | 21 | 1.2 | 11 | 1.2 | 32 | 1.1 |
| iSGLT-2 | 9 | 9.1 | 264 | 15.1 | 145 | 16 | 418 | 15.1 |
| iDPP-4 | 12 | 12.2 | 165 | 9.4 | 92 | 10.1 | 269 | 9.7 |
| arGLP-1 | 0 | 0 | 7 | 0.4 | 1 | 0.1 | 8 | 0.2 |
| Glinidas | 0 | 0 | 0 | 0 | 0 | 0 | 0 | 0 |
| Insulina | 30 | 30.6 | 487 | 27.8 | 267 | 29.4 | 784 | 28.4 |
| Monoterapia | 28 | 28.57 | 675 | 38.55 | 357 | 39.14 | 1060 | 38.39 |
| Doble terapia | 30 | 30.61 | 433 | 24.73 | 193 | 21.16 | 656 | 23.76 |
| Triple terapia | 10 | 10.20 | 261 | 14.91 | 155 | 17.00 | 426 | 15.43 |
| Tratamiento > 3 fármacos | 3 | 3.06 | 95 | 5.43 | 55 | 6.03 | 153 | 5.54 |
|
arGLP-1: agonista del receptor del péptido similar a glucagón; CV: cardiovascular; iDPP-4: inhibidores de la dipeptidilpeptidasa 4; iSGLT-2: inhibidores del cotransportador sodio-glucosa tipo 2; PPAR-y: agonista del receptor nuclear PPAR-y. |
||||||||
La asociación de las variables con el RCV muy alto mostraron una asociación significativa, la RACU 1.13 (RM: 1.13; IC 95%: 1.12-1.14; p < 0.00001), el IMC (RM: 1.09; IC 95%: 1.06-1.11; p < 0.00001) y la HbA1c (RM: 0.92; IC 95%: 0.86-0.98; p < 0.01) (Fig. 1).
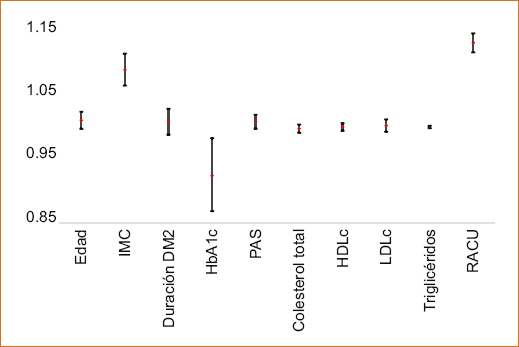
Figura 1. Análisis de factores asociados al riesgo cardiovascular. c-HDL: colesterol vinculado a lipoproteínas de alta densidad; c-LDL: colesterol vinculado a lipoproteínas de baja densidad; DT2: diabetes tipo 2; HbA1c: hemoglobina glucosilada; IMC: índice de masa corporal; PAS: presión arterial sistólica; RACU: relación albúmina: creatinina urinaria.
El modelo de recursos mínimos para predecir una TFGr mostró que el 57% de los sujetos está en riesgo de tener una TFG < 60 ml/min/m2, y que este riesgo está incrementado en aquellos sujetos que están en las categorías de RCV alto y muy alto (Fig. 2).
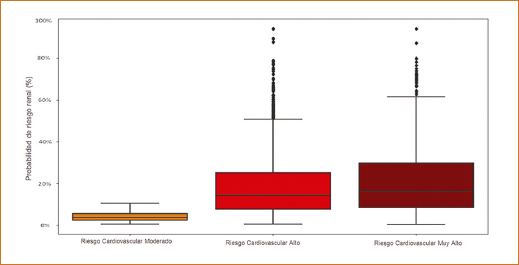
Figura 2. Probabilidad de presentar disminución de la tasa de filtrado glomerular. CV: cardiovascular.
Del subgrupo de pacientes con riesgo CV alto y muy alto (n = 2,663), se realizó ecocardiograma a 499 18.73%); en el 38% se reportó al menos alguna alteración, a pesar de que 454 (91%) se encontraban asintomáticos; el 4.6% reportó antecedentes de insuficiencia cardiaca. Los hallazgos ecocardiográficos estructurales fueron hipertrofia ventricular izquierda, en 105 casos (21%), crecimiento auricular izquierdo en 121 (24.2%) y disfunción diastólica en 34 (6.8%).
Discusión
En esta cohorte de pacientes con DT2 atendidos en el primer nivel de atención sin antecedentes de enfermedad cardiorrenal, se observó alta prevalencia de pacientes con alto y muy alto riesgo CV. En México existen pocos estudios que aborden el riesgo cardiorrenal en personas con DT2, por lo que los hallazgos de este estudio contribuyen a dimensionar las necesidades para poder llegar a los diferentes objetivos terapéuticos.
Las complicaciones cardiorrenales en la DT2 se han descrito en alrededor del 32 y 20% para ECV y ERC, respectivamente; estas se asocian con mayor riesgo de mortalidad4,17. En este estudio, utilizando el modelo de recursos mínimos desarrollado por Gendius como predictor de ERC se encontró en el 57%4,7. La presencia de albúmina en orina, además de ser un indicador de riesgo de progresión de enfermedad renal, también es indicador de daño endotelial, asociada a ECV ateroesclerótica e insuficiencia cardiaca. Por lo tanto, la RACU es un marcador mucho más temprano para identificar daño renal en pacientes con DT2 y constituye una herramienta diagnóstica muy útil que debería estar presente en el primer nivel de atención18,19.
Las alteraciones CV estructurales en pacientes asintomáticos con DT2 son importantes predictores de ECV y mortalidad20. Se ha reportado una prevalencia de hipertrofia del ventrículo izquierdo del 21.0%, crecimiento de aurícula izquierda (CAI) del 19.6% y disfunción diastólica del ventrículo izquierdo del 19.4%21. En esta cohorte, a los pacientes de alto/muy alto riesgo se les realizó un ecocardiograma, aunque estuvieron asintomáticos, y un pequeño porcentaje reportó datos compatibles con insuficiencia cardiaca, las alteraciones estructurales fueron similares en los dos grupos. El riesgo de un evento CV agudo incrementa significativamente en este grupo de personas22 y con ello, su impacto económico en los sistemas de salud. La identificación de las alteraciones estructurales CV o funcionales plantea la identificación de un grupo de pacientes de mayor riesgo CV, y por lo tanto candidatos a estrategias terapéuticas dirigidas para disminuir el riesgo de muerte CV23.
La prevalencia de otros FR asociados a ECV o renal en México se han incrementado24. Esta cohorte refleja la carga de FR en pacientes con DT2, la obesidad se asoció significativamente a mayor riesgo. La obesidad y la dislipidemia tienen un efecto aditivo en el desarrollo de ECV y ERC25. Importante mencionar que el grupo con alto/muy alto riesgo CV tenían menos de 10 años de diagnóstico de DT2, lo cual refleja la gran proporción de pacientes que cursan con un control subóptimo de los factores de riesgo cardiorrenal. Por esta razón, la identificación de manera temprana en la población mexicana y el tratamiento es el primer paso hacia la disminución de la morbimortalidad cardiorrenal17. Estos resultados plantean la necesidad de diseñar políticas de salud dirigidas a promover estilos de vida saludable, así como a identificar y tratar de manera oportuna estos factores de riesgo26,27.
Diferentes guías internacionales recomiendan la estratificación del riesgo cardiorrenal con la intención de ofrecer tratamiento oportuno centrado en las características de cada paciente. En los últimos años, terapias farmacológicas como los iSGLT2 y los arGLP-1 han demostrado disminuir el riesgo de muerte CV, infarto no fatal y enfermedad cerebrovascular, así como retrasar la progresión de la enfermedad renal12,13,28. El control integral de las cifras de glucemia, de presión arterial y de colesterol está asociado a un menor riesgo de mortalidad, incluyendo la mortalidad CV, en personas con DT229. La atención integral de personas con diabetes en México ha demostrado mejorar la posibilidad de que las personas alcancen los objetivos de la atención planteados por la Organización Mundial de la Salud, si bien el acceso a estos esquemas de atención sigue siendo limitado30. Finalmente, este estudio permite demostrar que existe una gran área de oportunidad en pacientes con riesgo alto/muy alto riesgo cardiorrenal, ya que un pequeño porcentaje de los participantes estaba recibiendo un iSGLT-2 o un arGLP-1.
El diseño transversal del estudio limita el establecimiento de la causalidad sin una duda razonable. Otra limitación son los datos autorreportados que podrían ser sujeto de sesgo de recuerdo o de deseabilidad social. Sin embargo, siempre que fue posible se cruzaron estos datos con los reportados en las pruebas diagnósticas clínicas, bioquímicas y de gabinete.
Conclusiones
Nuestros datos muestran que la población de primer nivel de atención que vive con DT2 tiene un alto/muy alto riesgo CV, aun estando asintomáticos, con menos de 10 años de diagnóstico y sin antecedentes de enfermedad cardiorrenal previa. La gestión temprana del riesgo permitirá priorizar los recursos diagnósticos y establecer un abordaje terapéutico personalizado con intervenciones multifactoriales sobre otros FR cardiorrenal como la HTA, obesidad o dislipidemias y con el uso de fármacos antidiabéticos con beneficio cardiorrenal (iSGLT-2 o arGLP-1) como lo recomiendan las guías internacionales y nacionales. Es necesario incrementar la conciencia sobre la relevancia de identificar de manera oportuna y prevenir complicaciones cardiorrenales en la DT2, así como acerca de la necesidad del diseño de políticas públicas que incluyan un abordaje integral de las personas con DT2, que incluya la gestión del riesgo cardiorrenal en el primer nivel de atención.
Financiamiento
Los autores declaran que este trabajo se realizó con recursos propios.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. Los autores han obtenido la aprobación del Comité de Ética para el análisis de datos clínicos obtenidos de forma rutinaria y anonimizados, por lo que no fue necesario el consentimiento informado.
Se han seguido las recomendaciones pertinentes. Declaración sobre el uso de inteligencia artificial. Los autores declaran que no utilizaron ningún tipo de inteligencia artificial generativa para la redacción de este manuscrito.
