Introducción
En la última década se ha reportado una prevalencia de enfermedad renal crónica (ERC) del 12.2% en la población general y 51.4 muertes por cada 100,000 habitantes en México, siendo la principal causa de mortalidad en pacientes con ERC la enfermedad cardiovascular, con un incremento del riesgo de hasta 20 veces respecto a la población general, incluso en estadios iniciales; hasta un 80% de los pacientes con ERC presentan enfermedad cardiovascular asociada1,2. Esta situación destaca la importancia de identificar la relación entre la ERC y el aumento del riesgo de calcificación vascular, dado que las complicaciones cardiovasculares son la principal causa de morbimortalidad en estos pacientes. Por ello, es esencial detectar biomarcadores precoces que permitan prevenir dichas complicaciones. En este sentido, Klotho es una proteína pleiotrópica que actúa como factor paracrino y endocrino en múltiples órganos, desempeñando así un papel clave en el metabolismo mineral, ya que se ha vinculado con procesos procalcificantes. No obstante, su función como indicador temprano de calcificación vascular en individuos con ERC está aún en fase activa de investigación3,4. Las funciones de la proteína Klotho y su relación con la progresión de la ERC y complicaciones cardiovasculares se describen en la tabla 15–36.
Tabla 1. Funciones de la proteína Klotho en distintos sistemas y órganos
| Sistema/órgano | Tipo de Klotho | Función principal | Mecanismo de acción | Implicación fisiopatológica | Referencias | ||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Sistema cardiovascular | α-Klotho | Regulación de la presión arterial (eje RAAS) Efecto antioxidante Homeostasis calcio y fósforo |
Inhibición de transformación de células musculares lisas Reducción de estrés oxidativo Bloqueo de canal TRPC6 |
Hipertensión arterial Calcificación vascular Daño miocárdico |
5–11 | ||||||
| Riñón | α-Klotho (s) | Regulación de metabolismo de fosfato y vitamina D (eje FGF23) Efectos nefroprotectores: antioxidante, antiinflamatorio, antifibrótico |
Transmembrana: correceptor de FGF23 Soluble: inhibición de TGF-β1 y Wnt/β-catenina, protección tubular |
Progresión de ERC Hiperfosfatemia Fibrosis renal |
12–21 | ||||||
| Hueso | α-Klotho | Regulación de metabolismo óseo mediante vía FGF23 Control de la síntesis de calcitriol |
Formación de complejo FGFR1-αKlotho Inhibición de reabsorción de fósforo (NaPi-2) Activación vía ERK1/2 |
Alteraciones en la homeostasis de vitamina D y fósforo Retraso en el crecimiento |
22–24 | ||||||
| Sistema endocrino | α-Klotho | Regulación en señalización de vía insulina/IGF-1 | Inhibición de autofosforilación de receptores de insulina | Diabetes tipo 2 Hipotiroidismo Retinopatía diabética |
25–27 | ||||||
| Hígado y tejido adiposo | β-Klotho | Regulación del metabolismo hepático y energético Regulación del apetito |
Formación de complejo con FGFr4 (FGF19): síntesis de ácidos biliares Complejo con FGFR1c (FGF21): metabolismo energético |
Resistencia a FGF19/FGF21 Alteraciones metabólicas en hígado Sarcopenia en cirrosis |
18,26,28,29 | ||||||
| Piel, ojo, sistema nervioso | γ-Klotho α-Klotho | Neuroprotección Integridad retiniana Regulación de envejecimiento cutáneo |
Expresión de PF4 en SNC Regulación de vías antioxidantes Inhibición de Wnt/β-catenina y TGF-β1 | Enfermedades neurodegenerativas Degeneración macular Retinopatía diabética |
13,30–33 | ||||||
| General | sKlotho | Regulación de envejecimiento y participación en múltiples sistemas | Correceptor para FGF23, FGF19, FGF21 Activación de vías de señalización Modulación de estrés oxidativo y apoptosis |
Envejecimiento acelerado Participación en múltiples enfermedades metabólicas |
13,19,31,34–36 | ||||||
|
ERC: enfermedad renal crónica; FGF: factor de crecimiento de fibroblastos; FGFR1: receptor de FGF tipo 1; IGF-1: factor de crecimiento similar a la insulina tipo 1; RAAS: sistema renina-angiotensina-aldosterona; SNC: sistema nervioso central; TGF-β1: factor de crecimiento transformador β1. |
|||||||||||
En esta revisión se incluyen la evaluación de la estructura molecular de Klotho, su relación con la progresión de la ERC y su potencial uso como biomarcador.
Bases moleculares de Klotho
En 1997, se codificó el gen de la proteína Klotho, siendo identificado como un gen antienvejecimiento. Klotho es una proteína pleiotrópica que actúa como factor paracrino y endocrino en múltiples órganos; es una proteína transmembrana y de cadena única que consta de 1012 aminoácidos. El dominio extracelular de Klotho puede escindirse mediante secretasas y posteriormente liberarse a la circulación en su forma soluble (sKlotho), la cual funciona como un factor humoral y ejerce múltiples efectos citoprotectores, tales como la supresión de factores proinflamatorios, el estrés oxidativo y la fibrosis, teniendo así un papel protector. El locus génico de Klotho en modelos murinos se encuentra en el cromosoma 5 y está rodeado por PDS5B y STARD13. El locus del gen de Klotho en el cromosoma 12 de los modelos murinos y en el cromosoma 13 humano es sinténico (localizado en el mismo cromosoma), ya que los genes vecinos son iguales en ambas especies. Existen cinco exones y cuatro intrones en la codificación del gen de Klotho en humanos y modelos murinos, que transcriben los nucleótidos de RNAm 3036 y 3042, respectivamente37. Las principales formas de la proteína Klotho, tanto transmembrana, como soluble, así como sus funciones más relevantes, se ilustran en la figura 1.
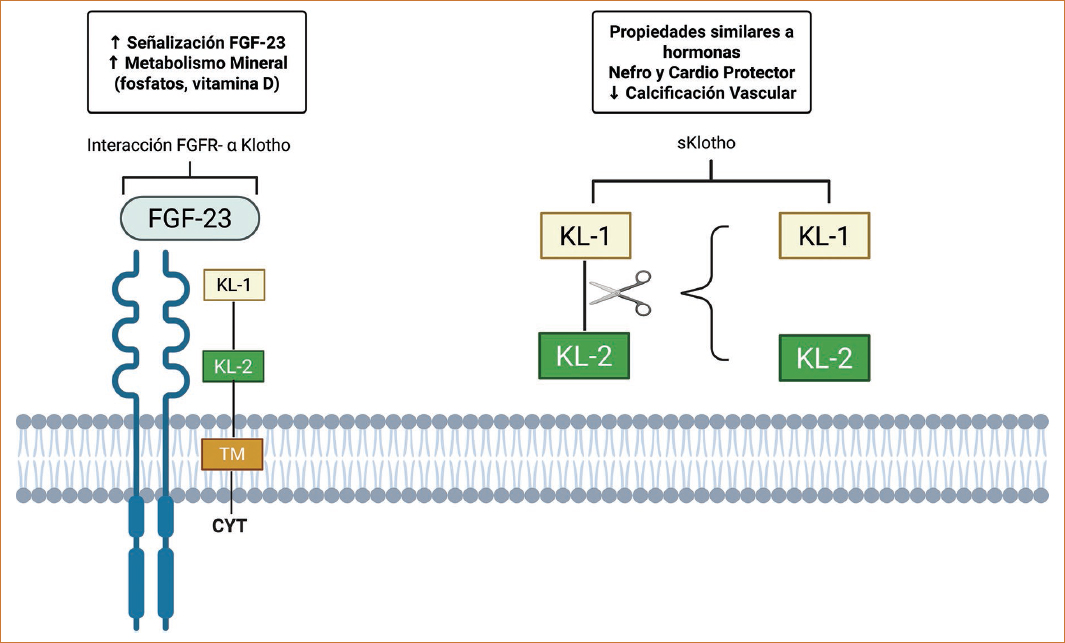
Figura 1. Formas principales de la proteína αKlotho y sus funciones. A la izquierda se observa la forma transmembrana de αKlotho, que actúa como correceptor para el receptor de factor de crecimiento de fibroblastos (FGF-R), facilitando su unión con FGF-23. Este complejo se caracteriza por la regularización del metabolismo del calcio y la vitamina D en órganos como el riñón. A la derecha se muestran las dos formas solubles de α-Klotho (sKL), resultantes del procesamiento proteolítico de la forma membranosa. Estos dominios (KL1 y KL2) poseen funciones similares a las de las hormonas circulantes, con funciones pleiotrópicas, incluyendo la protección antioxidante y la modulación de múltiples vías de señalización celular. CYT: región citoplasmática corta; TM: dominio transmembrana.
Hay cuatro grupos de proteínas Klotho que comparten una homología significativa: αKlotho, βKlotho, proteína relacionada con Klotho (klrp, una proteína citosólica β glucocerebrosidasa posiblemente implicada en la patogénesis de la enfermedad de Gaucher) y klph (Klotho lactase-phlorizin hydrolase, también llamada γKlotho), expresados en el tejido adiposo, los riñones, los ojos y la piel. La proteína Klotho muestra un patrón de expresión segmenterario en el riñón, con niveles elevados en el túbulo distaly niveles marcaamente reducidos en el túbulo proximal38,39.
Expresión tisular y regulación
La proteína Klotho se expresa predominantemente en los túbulos contorneados distales del riñón, y en menor medida en otros tejidos como el cerebro, el páncreas, las glándulas paratiroides y los vasos sanguíneos humanos. Se presenta en dos formas: transmembrana (mKlotho) y sKlotho, ambas derivadas de α-Klotho, la subfamilia más estudiada de esta familia de proteínas40. La forma mKlotho funciona como correceptor del factor de crecimiento fibroblástico 23 (FGF23) y es esencial para el mantenimiento de la homeostasis del fosfato y el metabolismo de la vitamina D, mientras que sKlotho actúa como hormona circulante con funciones antiinflamatorias, antioxidantes y antifibróticas41.
Subtipos de Klotho: α-Klotho, β-Klotho y γ-Klotho
α-Klotho se expresa altamente en el riñón, el plexo coroideo, las glándulas paratiroides y el nodo sinusal, así como en los sistemas nervioso, respiratorio, digestivo y reproductivo en distintos grados. Está compuesto por dos dominios extracelulares (KL1 y KL2), un segmento transmembrana y una corta cola citoplasmática no señalizante; la actividad y la función de α-Klotho están reguladas por estos dos dominios42. La forma de Klotho unida a la membrana constituye un complejo con los receptores del factor de crecimiento de fibroblastos 1c (FGFR1c), FGFR3c, FGFR4 y FGFR23, el cual desempeña un papel importante en la regulación de la secreción de paratohormona (PTH) y en la homeostasis del calcio, actuando a través del cotransportador Na+/K+-ATPasa en el plexo coroideo42. Entre sus principales acciones, se encuentran las siguientes:
- – Inhibición de la expresión de cotransportadores Na+/P tipo II en el túbulo proximal, lo que disminuye la reabsorción tubular de fosfato y favorece su eliminación urinaria.
- – Regulación negativa del metabolismo de la vitamina D, al disminuir la concentración de calcitriol, suprimiendo la actividad de la 1α-hidroxilasa (enzima que activa la vitamina D) y aumentando la degradación del calcitriol al estimular la 24-hidroxilasa43, a su vez afectando en la disminución de la expresión de los receptores de vitamina D y calcio de las glándulas paratiroideas. Ello incluye la mejora del estrés oxidativo y la inhibición de vías de señalización del factor de crecimiento de insulina, Wnt/β-catenina, factor de crecimiento transformador β1 (TGF-β1), y la inhibición de la señalización de rapamicina (vía mTOR). Además, α-Klotho puede encontrarse en plasma debido a la escisión de la porción extracelular dependiente de proteasas (α-Klotho soluble) o bien por la producción y liberación de un ectodominio competo (α-Klotho secretado).
La forma α-Klotho soluble es capaz de aumentar la densidad transmembrana de los transportadores TRPV5 (miembro de la subfamilia V del canal de potencial transitorio) y ROMK1 (canal de potasio medular externo renal). Esta actividad se encuentra regulada por la actividad sialidasa de Klotho, que se encarga de hidrolizar los ácidos siálicos enlazados en los sitios 2,6 de N-glicosilación de TRVP5 y ROMK1. Siendo ambas proteínas canales importantes para la reabsorción de Ca2+ y K+ en la membrana de las células epiteliales renales, la hidroxilación impide la internalización de TRVP5 y ROMK1. α-Klotho forma un complejo receptor ternario con los receptores FGFR1c, FGFR3c, FGFR4 y FGF23, mediando el equilibrio del metabolismo del calcio y del fósforo, así como la producción de vitamina D activa en el cuerpo. β-Klotho se expresa principalmente en el hígado y en el tejido adiposo blanco (páncreas, cerebro), donde puede formar complejos con FGFR1c y FGFR4 y activar vías de señalización intracelular. γ-Klotho tiene solo un dominio estructural extracelular similar a la β-glucosidasa y una corta región de cola citoplasmática, y se expresa principalmente en el riñón, la grasa parda, la piel y los ojos. Tras unirse a FGFR1b, FGFR1c y FGFR2c, se convierte en un receptor de alta afinidad para el complejo FGFR4/FGF1942. La expresión de Klotho disminuye con la edad, lo que afecta a la homeostasis ósea y promueve el envejecimiento. Klotho regula vías clave como el FGF23, el factor de crecimiento similar a la insulina tipo 1 (IGF-1) y Wnt (factores de señalización tisular Int-1), influyendo en el equilibrio electrolítico, el estrés oxidativo y la proliferación celular44. Klotho bloquea la activación de Wnt al unirse a varios ligandos, como Wnt1, Wnt3, Wnt4 y Wnt5a. En ratones deficientes en Klotho, el exceso de activación de Wnt promueve la senescencia celular y tiene un impacto negativo en la supervivencia de las células madre. En el riñón, la sobreexpresión y la cooperación entre Wnt y TFG-β induce la transición epitelial-mesenquimal, que es un precursor de la fibrosis y del cambio de fenotipo endotelial41.
Fisiopatología de la deficiencia de Klotho en la enfermedad renal
En el contexto de la ERC, diversos estudios han mostrado una reducción progresiva de la expresión de Klotho, correlacionada con una disminución de la tasa de filtración glomerular estimada (TFGe). Esta regulación negativa está impulsada por mecanismos tanto epigenéticos como no epigenéticos. La inflamación crónica, común en la ERC, inhibe la transcripción del gen de Klotho mediante la metilación de su promotor, la desacetilación de histonas y la acción de micro-ARN y ARN largos no codificantes. También contribuyen factores no epigenéticos, como el estrés del retículo endoplásmico y la degradación de proteínas intracelulares45. El FGF23 y Klotho desempeñan un papel primordial en la regulación mineral ósea, y sus alteraciones secundarias a las ERC, inhibiendo el TGF-β, el IGF-1, el factor nuclear kappa B y la Wnt/β-catenina46. El FGF23 es sintetizado por los osteocitos como una molécula de 251 aminoácidos. El cofactor Klotho es necesario para la unión de este receptor, lo que permite la reabsorción de fosfato en los túbulos proximales renales. El FGF23 regula la 1-α-hidroxilasa, el fosfato sérico y la PTH. En condiciones fisiológicas normales, el FGF23 circulante se une a los complejos del FGFR1–α-Klotho (KL) en la membrana basolateral de las células del túbulo proximal renal. Esta unión activa la cascada de señalización de MAPK, que involucra a ERK1 y ERK2, y conduce a la internalización y la degradación de NPT2a y NPT2c, lo que resulta en una disminución de la reabsorción urinaria de fosfato y su consiguiente pérdida. La señalización de FGF23 en el túbulo proximal también induce mecanismos posteriores que suprimen la transcripción de la vitamina D 1α-hidroxilasa (CYP27B1) y aumentan la transcripción de la vitamina D 24-hidroxilasa (CYP24A1)47. Debido a la relación directa con el FGF23, Klotho desencadena su principal acción: reducir la reabsorción de fosfato en los riñones. Su secreción por las células óseas se produce al aumentar la concentración de fosfato, desempeñando un papel importante en la homeostasis del fosfato al disminuir la reabsorción de este en los túbulos renales y aumentar su excreción48. Además, la expresión de Klotho se modula a través del FGF23, siendo Klotho un elemento esencial para la acción renal de FGF23. La expresión de Klotho disminuye conforme se reduce la TFGe, lo que altera la señalización de FGF2349. En las etapas tempranas de la ERC, el FGF23 incrementa la fosfaturia, previniendo la acumulación de fosfatos; este proceso requiere una correcta producción de Klotho, y por lo tanto su deficiencia conduce a un estado de resistencia a FGF23, causando daño orgánico al corazón, el endotelio y el hueso48. Varios estudios han demostrado que la excreción urinaria de proteína Klotho disminuye en las primeras etapas de la ERC50; los niveles séricos de Klotho son progresivamente más bajos a medida que se pierde la función renal, con una disminución media ajustada de 3,2 pg/ml por cada disminución de 1 ml/min/1,73 m2 de la TFGe51. Sin embargo, conforme hay progresión de la ERC, los niveles de FGF23 aumentan de manera exponencial, y la baja expresión y la falta de Klotho en el cuerpo limitan el efecto del FGF23 en la regulación del fósforo en sangre52. La relación entre FGF23, calcitriol y fósforo, dependiente de la presencia de Klotho como correceptor en el tùbulo renal, se resume en la figura 2, donde se resume su relevancia en la homestasis mineral en la ERC.Estudios recientes destacan la existencia de una retroalimentación positiva entre el FGF23 y citocinas proinflamatorias como la IL-6, el TNFα y la proteìna C reactiva en los pacienes con ERC. Este circuito es relevante porque el FGF23, más allá de su función principal como regulador del fósforo producido por células óseas (osteocitos y osteoblastos), actúa formando un complejo ternario con un receptor de FGF y la proteína Klotho. La interacción con citocinas sugiere un vínculo importante entre la inflamación y el metabolismo mineral en la ERC. El hiperparatiroidismo secundario es una de las complicaciones metabólicas más comunes derivadas de la ERC. El FGF23 y la proteína Klotho son los factores cuyas concentraciones cambian más temprano en el desarrollo de hiperparatiroidismo secundario. Las principales y más peligrosas complicaciones de este involucran los sistemas esquelético y cardiovascular. El aumento de la PTH relacionado con la ERC puede estimular la secreción de FGF23 a través de Nurr1 (Nuclear receptor related 1 protein). En el hiperparatiroidismo, hipotéticamente, FGF23 quedaría suprimido, ya que la hipersecreción de PTH causaría hipofosfatemia y se eliminaría uno de los estímulos de secreción de FGF2353. La consecuencia del hiperparatiroidismo secundario es la aparición de trastornos minerales y óseos, que incluyen osteodistrofia renal y calcificaciones en los vasos sanguíneos que conducen a complicaciones cardiovasculares54. En un modelo experimental se observó una relación directa entre los niveles de Klotho y la rigidez arterial, y se ha demostrado que la presencia de Klotho tiene un impacto positivo contra la calcificación vascular previniendo la transformación de células vasculares a células similares a osteoblastos55. También se ha observado que Klotho ejerce un efecto cardioprotector directo, especialmente frente a la hipertrofia ventricular izquierda. En estudios con ratones hipomórficos para el gen de Klotho se vio que la deficiencia de esta proteína se asocia con mayor fibrosis miocárdica, hipertrofia ventricular izquierda y reducción de la fracción de eyección, especialmente en presencia de ERC. La administración exógena de Klotho soluble mejoró estos parámetros de disfunción miocárdica de manera independiente del fósforo, el FGF23, la presión arterial y el filtrado glomerular. El efecto cardioprotector de Klotho se vincula con la inhibición del canal de calcio TRPC6, cuya sobreexpresión en la uremia favorece la entrada de calcio intracelular, activación de la vía calcineurina-NFAT y expresión de genes fetales, promoviendo un remodelado patológico e hipertrofia ventricular izquierda. Al bloquear esta vía, Klotho emerge como una prometedora estrategia terapéutica para mitigar el daño cardiaco en los pacientes con ERC50.
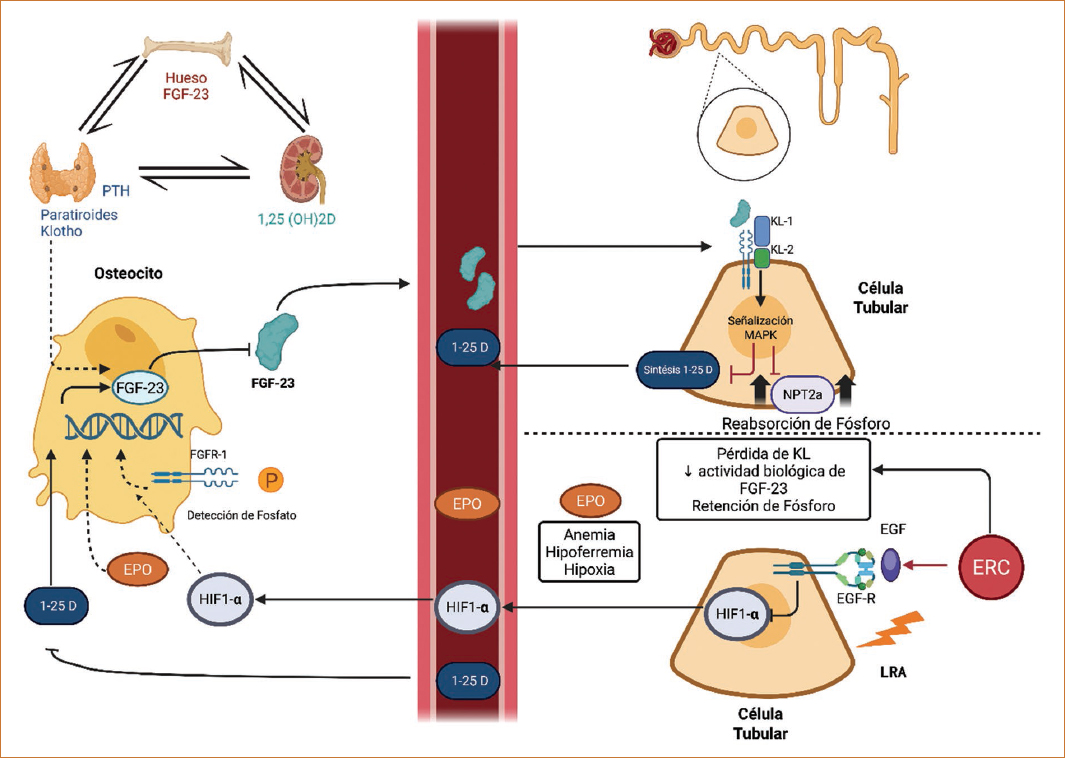
Figura 2. Relación del factor de crecimiento de fibroblastos 23 (FGF23) con el calcitriol y el fósforo. La acción de FGF23 en el sistema renal depende de su unión al receptor FGFR-1 y a la proteína Klotho, que actúa como correceptor en la membrana tubular renal. Esta unión activa la señalización MPAK, promoviendo la síntesis de calcitriol (1,25(OH)2D) y la reabsorción de sodio a través del cotransportador NPT2a. EGF: factor de crecimiento epidérmico; EGF-R: receptor de EGF; EPO: eritropoyetina; HIF-1α: factor inducible por hipoxia 1-alfa; MAPK: proteína cinasa activada por mitógenos; NPT2a: cotransportador de sodio-fósforo tipo 2a; PTH: hormona paratiroidea.
Implicaciones clínicas y terapéuticas
En un estudio se asoció la función renal con el nivel de Klotho en una cohorte de adultos de 70-79 años con una TFGe media de 73 ml/min/1.73 m2, y se encontró una asociación entre el incremento de sKlotho y la disminución en el riesgo de deterioro de la función renal durante 10 años, aun después de ajustar los datos demográficos, incluyendo al FGF23 (odds ratio [OR] 0.78 e intervalo de confianza del 95 [IC 95%] de 0.66-0.93 para un deterioro del 30% en la TFGe, y OR de 0,85 e IC 95% de 0.73-0.98 para un deterioro > 3 ml/min por año en la TFGe), pero no de ERC incidente (cociente de tasas de incidentes de 0.90 e IC 95% de 0.78-1.04)56,57.
Este estudio evaluó a 236 pacientes que se sometieron a una biopsia renal por ERC y se observó que los niveles de Klotho sérico en aquellos en HD de mantenimiento eran deficientes en α-KL renal, y que eran significativamente menores que en pacientes pre-HD con ERC en estadio 5 (HD 383.1 ± 179.9 pg/ml y pre-HD 495.6 ± 181.9 pg/ml; p < 0.05). Estos resultados sugieren que los niveles de sKL podrían ser un marcador útil de los niveles renales de a-KL58. En un estudio clínico con una cohorte de 68 pacientes (edad 58 ± 15 años; TGFe 45 ± 21 ml/min) se analizaron los niveles de s-Klotho sérico y FGF23 sérico, y se observó una inferioridad en s-Klotho (519 ± 183 frente a 845 ± 330 pg/ml; p < 0.001) en los pacientes renales, detectable desde el estadio 2 de la ERC (p < 0.001), mostrando una correlación positiva de s-Klotho con la TGFe59. En un análisis transversal, los niveles séricos más bajos de α-Klotho se asociaron con un estadio más grave de ERC. Al clasificar en dos grupos a los pacientes según el valor basal medio de α-Klotho, 43 (35.2%) pacientes con niveles de α-Klotho ≤ 396.3 pg/ml alcanzaron el resultado compuesto primario en comparación con 19 (15.7%) con niveles de α-Klotho > 396.3 pg/ml (hazard ratio: 2.03; IC 95%: 1.07-3.85; p = 0.03)60. En estudios clínicos de inmunohistoquímica se ha reportado que la expresión de Klotho se reduce gravemente en pacientes con ERC a medida que avanza el estadio, debido al deterioro funcional de las células del túbulo contorneado61. A pesar de ello, no existe un consenso definitivo en los estudios clínicos previos para la evolución temporal de las variaciones séricas de sKlotho en la ERC, siendo las primeras limitantes la estadificación de la ERC y la forma de procesamiento de las muestras (ELISA), con diversos tipos de muestras, calidad, métodos de recolección, procesamiento, condiciones de almacenamiento y ciclos de congelación-descongelación. En síntesis, las limitaciones entre el sKlotho sérico y el urinario se deben a la falta de estudios en los que se evalúe la relación entre sus niveles y el grado de afección renal56,62.
Discusión
La presente revisión trata de demostrar el papel central que posee la proteína Klotho, la cual funciona como un regulador de múltiples sistemas y cuya deficiencia no se debe únicamente a la ERC, sino que actúa como un actor clave para la progresión de esta y funge como adyuvante para la aparición de comorbilidad. Los hallazgos en los diferentes estudios y análisis sugieren que la pérdida progresiva de Klotho desde los estadios iniciales de la ERC es un detonante que acelera la disfunción de diferentes mecanismos, tales como disregulación mineral, inflamación, estrés oxidativo y daño cardiovascular. Existe una relación íntima entre Klotho y FGF23 que es necesaria explorar para entender su papel en la ERC. En las fases tempranas, el sistema Klotho-FGF23 funciona como un mecanismo compensador para promover la excreción de fosfato, induciendo fosfaturia; sin embargo, la disminución progresiva de Klotho conduce a una resistencia en los mecanismos de acción de FGF23, desencadenando hiperfosfatemia e hiperparatiroidismo secundario, y finalmente traduciéndose en un trastorno mineral óseo asociado a ERC. Estas consecuencias no afectan únicamente al riñón y al hueso, pues la evidencia indica que la deficiencia de Klotho crea un ambiente que propicia alteraciones vasculares (calcificación) e incluso fibrosis miocárdica, explicando en gran parte el alto riesgo cardiovascular que cargan estos pacientes. Klotho ha surgido no solo como un marcador, sino también como una molécula con efectos que pueden ser considerados protectores. Su capacidad para inhibir vías proinflamatorias y profibróticas, tales como TGF-β y Wnt/β-catenina, así como su acción directa en canales iónicos como TRPC6, los cuales ayudan a prevenir la hipertrofia ventricular, posicionan a esta proteína como una diana terapéutica con un potencial enorme, tal como se ha demostrado en modelos experimentales. La administración exógena de sKlotho en modelos experimentales ha demostrado mitigar el daño miocárdico y vascular independientemente de otros factores, abriendo la puerta a futuras investigaciones e intervenciones que podrían cambiar el curso natural de la enfermedad. Sin embargo, aún estamos lejos de poder trasladar estos hallazgos a la práctica clínica, debido a la falta de consenso sobre los niveles séricos de Klotho, lo cual permitiría utilizarlo como un marcador, por lo que se deberían establecer protocolos estandarizados con la finalidad de utilizar Klotho, además de como un marcador pronóstico, como una herramienta que permita estratificar el riesgo y monitorizar a los pacientes que se encuentren en alto riesgo.
Conclusión
La proteína Klotho surge como un marcador pronóstico dentro del panorama de la ERC, siendo su deficiencia un marcador en la ERC, y por otro lado contribuye a la enfermedad mineral ósea y al deterioro cardiovascular. Lograr comprender su fisiopatología permitiría entender la comunicación que existe entre el riñón, el hueso y el sistema cardiovascular. La evidencia actual sugiere que preservar o buscar restaurar los niveles de Klotho podría, por un lado, frenar la progresión de la enfermedad renal, y por otro, proteger al sistema cardiovascular y evitar complicaciones que en los pacientes con ERC son la primera causa de mortalidad. Aún queda mucho por investigar y se requiere una estandarización de los métodos de investigación con la finalidad de validar su utilidad clínica y explorar terapias seguras y efectivas. Sin embargo, entender el papel crucial de Klotho permite dar un paso más hacia un estudio nefrológico más predictivo, preventivo y personalizado, con el objetivo de mejorar la calidad y la esperanza de vida de los pacientes con ERC.
Financiamiento
Los autores declaran que este trabajo se realizó con recursos propios.
Conflicto de intereses
Los autores declaran no tener conflicto de intereses.
Consideraciones éticas
Protección de personas y animales. Los autores declaran que para esta investigación no se han realizado experimentos en seres humanos ni en animales.
Confidencialidad, consentimiento informado y aprobación ética. El estudio no involucra datos personales, historias clínicas ni muestras biológicas humanas, por lo que no requiere aprobación ética. No se aplican las guías SAGER.
Declaración sobre el uso de inteligencia artificial (IA). Los autores declaran que no se utilizó ningún tipo de inteligencia artificial generativa para la redacción ni la creación de contenido de este manuscrito.
